تشخیص زودهنگام آلزایمر با کمک طیفسنجی فروسرخ و امضای مولکولی

در این پست، متن گفتگویی را میخوانید که با خانم دکتر سینتا مکموری در خصوص آخرین تحقیقات او در زمینه بیماری آلزایمر صورتگرفته است. او اخیراً موفق به توسعه یک تکنیک امضای مولکولی شد که میتواند به تشخیص زودهنگام آلزایمر (قبل از بروز علائم بیماری) کمک کند.
بیماری آلزایمر ششمین عامل مرگومیر در کشور آمریکا است و سالانه زندگی میلیونها نفر در سراسر جهان را تحتتأثیر قرار میدهد. چه چیزی الهامبخش آخرین تحقیقات شما در مورد بیماری آلزایمر شد؟
آلزایمر یکی از مشکلات عمده در جهان است و ۲ درصد از مردم آمریکا در دهه آینده به آن مبتلا خواهند شد. میزان ابتلا به این بیماری روندی صعودی دارد زیرا ما به راهی برای تشخیص آن دست پیدا نکردهایم. همچنین، هیچ درمان یا روشی برای تشخیص آلزایمر وجود ندارد و این بیماری مبتنی بر هیچ عامل ژنتیکی نیست.
بنابراین، این سؤال برای من پیش آمد که چه عاملی در همه مبتلایان به این بیماری مشترک است؟ وقتی چیزی در مورد این عامل مشترک نمیدانیم، چگونه میتوانیم این مشکل را حل کنیم؟ من میخواستم بررسی کنم که آیا این افراد از نظر شیمیایی به هم شباهتی دارند یا خیر. شیمی زیربنای فیزیولوژی است؛ بنابراین، اگر شما شخصی را درمان کنید، از شیمی بدن او استفاده کردهاید. من چنین نظری داشتم و هدف من بررسی عوامل شیمیایی مشترک موجود در بین جمعیت زیادی از بیماران مبتلا به آلزایمر و رسیدن به نشانهای از نحوه واکنش بدن آنها به درمانها بود.
در حال حاضر روند تحقیقات و درمان این بیماری چگونه است؟ آیا محدودیتی برای درمان وجود دارد؟
هیچ درمانی برای آلزایمر وجود ندارد. در طول این سالها حدود ۱۵۰ آزمایش بالینی ناموفق انجام شده است. اخیراً یک آنتیبادی برای بیماری آلزایمر ساخته شد که توسط FDA تأیید شده است، اما تأثیر این آنتیبادی هنوز مشخص نیست.
حتی اگر چیزی ندانیم، میتوانیم از این تکنیک برای پیگیری روند بیماری و بهبود آن استفاده کنیم. در حال حاضر، هیچکس واقعاً نمیداند چه زمانی باید درمان بیمار را شروع کند و چه زمانی آن را متوقف کند.
در حال حاضر، حتی تشخیص بیماری آلزایمر یک شخص، هم برای خود بیمار و هم برای خانواده او سودمند است. آنها میتوانند به فکر استخدام پرستار بیفتند. همچنین، بیماران میتوانند رژیمهای غذایی را شروع کنند که برای آنها مناسبتر است. آگاهی از این بیماری فواید زیادی دارد.
در حال حاضر، تشخیص بیماری آلزایمر در مراحل اولیه آن دشوار است. چرا اینگونه است و مزایای تشخیص زودهنگام این بیماری چه هستند؟
معمولاً [دشوار بودن تشخیص بیماری] بهاینعلت است که علائم آشکار آن بسیار خفیف هستند. برای مثال، فراموشی را در نظر بگیرید. احتمالاً بین خویشاوند شما یک فرد فراموشکار وجود داشته باشد. فراموشکاری یکی از فنوتیپ [یا صفتهای عادی] افراد است. این که آن را به آلزایمر نسبت بدهیم کار دشواری است.
یکی دیگر از ویژگیهای آلزایمر پپتیدهای بتا است. در افراد عادی دو نوع از این پپتیدها تشکیل میشوند. یکی بد است و دیگری بهتر. ازآنجاکه این پپتیدها در افراد عادی نیز تشکیل میشوند، کمپلکسهای بتا نمیتوانند شاخصی برای ابتلا به بیماری آلزایمر در نظر گرفته شوند. حدود ۱۱ سال طول میکشد تا بیماری آلزایمر شروع به ایجاد فنوتیپهای قابلاندازهگیری کند. شاید غیرممکن نباشد، اما تشخیص این بیماری در مراحل اولیه بسیار دشوار است.
به دلیل دشوار بودن تشخیص اولیه یا پیشبینی آلزایمر، تهیه دارو برای آن نیز کار دشواری است. تحقیق جدید شما چگونه میتواند به تغییر این وضعیت کمک کند؟
یکی از رایجترین راهحلها [برای تشخیص این بیماری] توسعه شاخصهای زیستی است. شاخصهای زیستی مولکولهایی هستند که با بیماری تغییر میکنند و امکان ردیابی آنها وجود دارد. استفاده از این شاخصها مخصوصاً در بیماریهایی که منشأ آن را نمیدانیم موفقیتآمیز نبوده است. ممکن است این نشانگرها از فردی به فرد دیگر متفاوت باشد؛ بنابراین اغلب راهحل مفیدی به شمار نمیآید.
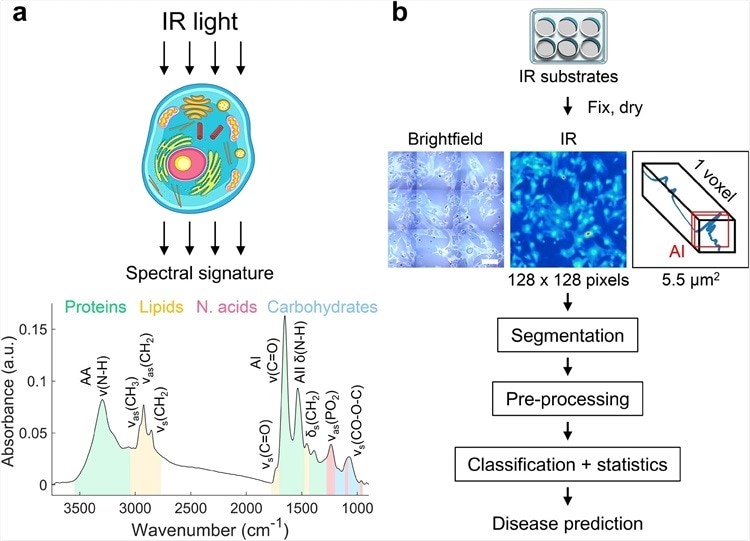
روش جدیدی که در مورد آن صحبت میکنیم یک شاخص زیستی نیست، بلکه به شما یک ”امضا“ در خصوص وضعیت شما و بیماری شما میدهد. تبدیل فوریه فروسرخ (FTIR) تمام مولکولهای موجود در سلول را اندازهگیری میکند. این طیفسنج آنقدر حساس است که دهها هزار مولکول موجود در سلول را مشخص میکند. هر سلول مقداری ترکیبات شیمیایی یکسان دارد، اما همه این ترکیبات به یکشکل کنار هم قرار نمیگیرند.
بنابراین، محصولات ژنی در یک سلول ممکن است با پروتئینهایی تعامل داشته باشند که کمی با هم تفاوت دارند و بنابراین سیگنالهای نسبتاً متفاوتی تولید میکنند. این دو فراورده ژنی با وجود یکسان بودن ترکیبات شیمیایی اولیه، واکنشهای متفاوتی دارند.
هدف ما پیگیری یک مولکول نیست. ما به مجموعه نگاه میکنیم و میانگین کاری که سلول انجام میدهد را بررسی میکنیم. اگر سلول جزو سلولهای بیمار باشد، متوجه ابتلای فرد به بیماری میشویم.
اگر امکان دارد در مورد آخرین تحقیقات خود در زمینه فنوتیپ طیفی و بیماری آلزایمر توضیح دهید؟
تحقیقات ما بر پایه یک روش محاسباتی بود. ما جهت بررسی، سلولها را میگرفتیم و سپس نور طبیعی به آنها میتاباندیم تا برانگیخته شوند. سلولها به نور واکنش نشان میدهند و ارتعاش خاصی تولید میکنند. سپس آن اطلاعات را جمعآوری میکردیم. هر یک از ارتعاشات یک فرکانس است و تمام سیگنالهای مختلف توسط دستگاه رصد میشوند.
ما الگوریتمی تعریف کردیم که این سیگنالها را به یک امضا یا علامت مشخصی تبدیل کند. در نتیجه این کار، مجموعهای از اطلاعات از میکروسکوپ به کامپیوتر میرود. کامپیوتر محاسباتی بر روی آن اطلاعات انجام میدهد و آنها را در قالب سیگنالی به ما میدهد.
شما چه کشفی کردید؟
یکی از مشکلات بیماریهای عصبی این است که هیچکس نمیتواند تا زمانی که زنده است مغز خود را اهدا کند. [خانم دکتر به این موضوع اشاره دارند که بیماریهای عصبی مغزی را معمولاً بعد از فوت فرد بیمار و کالبدشکافی مغز مطالعه میکنند.] این که شما بتوانید از یک سلول جایگزین و در دسترس استفاده کنید مزیت بزرگی به شمار میآید. ما نیازی به استفاده از بافت نداریم، تنها با چند سلول پوستی بر آنچه در مغز میگذرد نظارت میکنیم.
اگرچه سلولهای پوست سلولهای مغزی نیستند، اما ژنتیک مشابهی دارند. آنها به روش خود به بیماری واکنش نشان میدهند، پس میتوانند روند پیشرفت بیماری را مشخص کنند. این سلولها بهعنوان یک شاخص عمل میکنند و میتوانند در دستیابی به روند بیماری به ما اطلاعاتی بدهند.
یکی از تصورات اشتباهی که در مورد این فناوری وجود دارد این است که از آن برای آسیبشناسی استفاده میشود. باوجوداینکه ما میتوانیم این کار را بکنیم، اما در این مرحله انجام آن بیفایده است. هدف ما این بود که هر چه زودتر بر روی فرد زنده (بیماری) کاری انجام دهیم تا او شانس بیشتری داشته باشد. این روش برای تشخیص زودهنگام بیماری است و به نظر من اگر در میان جمعیتهای زیادی از این فناوری استفاده کنیم به قدرت بیشتری دست میابیم.
معمولاً از روشهای مبتنی بر شاخصهای زیستی در مطالعه بیماریهایی مانند بیماری هانتینگتون استفاده میشود. منظور شما از شاخص زیستی چیست و چرا این روش برای مطالعه بیماری آلزایمر اجرا نمیشود؟
هانتینگتون مثال کلاسیک یک نقص تک ژنی است. ما در درجه اول به همین دلیل این بیماری را مطالعه میکنیم. ما میدانیم که بهجز یک علت هیچ دلیل دیگری برای بروز این بیماری وجود ندارد. در نتیجه، میدانیم چه ژنی را هدف قرار دهیم و میتوانیم فوراً آن را تشخیص دهیم؛ بنابراین، مورد مناسبی برای استفاده از یک شاخص زیستی است.
در مورد بسیاری از بیماریهای مبتنی بر جهش این موضوع صادق است. شما میتوانید جهش را بررسی کنید و از یک شاخص زیستی ساده استفاده کنید.
سطح دوم شاخصهای زیستی صرفاً در مورد بررسی یک ژن نیست، بلکه در مورد ژنهای است که شما در طول زندگی بیمار آنها را ارزیابی میکنید. برای مثال، بسیاری از مواقع در بیماری سرطان شما میتوانید چند ژن که با پیشرفت سرطان تغییر میکنند را شناسایی کنید و به بررسی سیگنال آنها بپردازید.
بااینوجود، شما نمیتوانید گروه کوچکی از ژنها را انتخاب کنید و ادعا کنید بیماری را میشناسید. این ژنها هرگز منحصر به این بیماری نیستند. آنها ممکن است شاخص قدرتمندی باشند، اما بهاندازه کافی خوب نیستند. ممکن است شما به این نکته برسید که این ژن در سرطانهای دیگر دیده شده است، اما در درازمدت معنای خاصی ندارد.
با این که طیفسنجی فروسرخ (IR) در زمینههای مختلف علمی از جمله کشاورزی، علوم مواد و زمینشناسی استفاده میشود، چرا این روش در جامعه علوم پزشکی چندان محبوب نیست؟ آیا امیدوارید که تحقیقات شما کاربردهای فراوان IR را به دیگر افراد نشان دهد و آنها را به استفاده از این فناوری تشویق کند؟
دو دلیل وجود دارد. اول اینکه این روش در کشاورزی و سایر زمینهها استفاده میشود زیرا در این شاخهها هیچ تغییری رخ نمیدهد. اما در پزشکی، پزشک باید از آن برای تشخیص بیماری استفاده کند. لازم است که پزشکان احساس کنند که میتوانند روی این روش حساب کنند.
یکی از پرسشهای مردم این است که چگونه میشود از این روش برای همه بیماریها استفاده کرد. باید بگویم ارتعاشات مولکولها آنقدر حساس هستند که هرکدام سیگنال منحصربهفرد خود را میدهند. سؤال دیگر این است که آیا میشود با این تکنیک بیماریها را از یکدیگر تشخیص داد؟ در حال حاضر، ما در حال جمعآوری اطلاعات بیماریهای مختلف هستیم و تا زمان کامل شدن این اطلاعات نمیتوانیم در مورد نتیجه اظهارنظر کنیم.
منبع:
https://www.news-medical.net/news/20220111/Developing-a-fingerprint-test-that-could-diagnose-Alzheimere28099s-early.aspx





